Autor: Dr. Ing. Hartmut Junke
Fizyczne oczyszczanie wody jest przedmiotem badań wielu uczonych od ponad 20 lat.
Podczas tego czasu udowodniono jego skuteczność. Czasami jednak jest ona kwestionowana i odrzucana. Aby znaleźć tego przyczyny ważnym wydaje się być przeanalizowanie podstaw fizycznych, które pozwolą wyjaśnić sposób działania procesu/ów fizycznego oczyszczania wody i wyjaśnić sporne kwestie.
Istnieje wiele informacji dotyczących wysokiej skuteczności tego typu oczyszczania wody pochodzących od uznanych instytucji m. in. Instytut Fizjologii Uniwersytetu Ludwika Maksymiliana w Monachium. W tej instytucji, wymiana laserów rurowych spowodowana odkładaniem się kamienia kotłowego podczas chłodzenia okazała się być do uniknięcia dzięki zastosowaniu urządzenia do fizycznego oczyszczania wody. Uzyskane wyniki potwierdzają skuteczność wyżej wymienionej metody, jednakże kwestia braku spodziewanych efektów także bywa podnoszona. W większości przypadków zwykli użytkownicy nie znają nawet producenta urządzenia.
Po przeczytaniu publikacji naukowych również można odnieść wrażenie, że kwestionują one skuteczność tej metody, jednak często nie podają one żadnych dowodów naukowych uzasadniających krytykę fizycznego oczyszczania wody.
 Celem stosowania tego typu oczyszczania jest usuniecie kamienia kotłowego. Z chemicznego punktu widzenia kamień kotłowy to węglan wapnia (CaCO3). Jest to biała substancja krystaliczna, trudno rozpuszczalna w wodzie. Wytwarza się jednak w wodzie nasyconej tlenkiem węgla(IV) (przechodząc w wodorowęglan wapnia Ca(HCO2), co jest możliwe, gdyż dwutlenek węgla CO2 reaguje z wodą H2O tworząc kwas węglowy H2CO3) lub w roztworze chlorku amonu (przechodząc w chlorek wapnia). W wysokich temperaturach, a także pod wpływem kwasów ulega on rozkładowi z wydzieleniem dwutlenku węgla. W przyrodzie występuje w postaci minerałów: aragonitu i kalcytu (główny składnik wapieni, marmuru i kredy).
Celem stosowania tego typu oczyszczania jest usuniecie kamienia kotłowego. Z chemicznego punktu widzenia kamień kotłowy to węglan wapnia (CaCO3). Jest to biała substancja krystaliczna, trudno rozpuszczalna w wodzie. Wytwarza się jednak w wodzie nasyconej tlenkiem węgla(IV) (przechodząc w wodorowęglan wapnia Ca(HCO2), co jest możliwe, gdyż dwutlenek węgla CO2 reaguje z wodą H2O tworząc kwas węglowy H2CO3) lub w roztworze chlorku amonu (przechodząc w chlorek wapnia). W wysokich temperaturach, a także pod wpływem kwasów ulega on rozkładowi z wydzieleniem dwutlenku węgla. W przyrodzie występuje w postaci minerałów: aragonitu i kalcytu (główny składnik wapieni, marmuru i kredy).
Zatem nasuwa się pytanie: dlaczego wapno się wytrąca?
Stężenie rozpuszczonego Ca(HCO3)2 nigdy przecież nie osiąga wartości nasycenia, która, jeśli przekroczona, powodowałaby wytrącanie rozpuszczonej substancji w postaci krystalicznej? Odpowiedzi na to pytanie mogą udzielić miejsca, w których zarastają rurociągi. Są to przede wszystkim kolanka, rozgałęzienia i punkty końcowe (w tym również krany). Dzieje się to zwłaszcza tam, gdzie jest styczność z ciepłą wodą, ale zauważyć należy, że zbiorniki wody ciepłej są wolne od kamienia w przeciwieństwie do zawsze zakamieniałych powierzchni, które ogrzewają wodę.
Zatem, dlaczego w tych punktach osadza się kamień?
Odpowiedź jest bardzo prosta: musi być gradient/różnica energii która prowadzi do otwarcia struktur wodnych tzw. klatek dookoła rozpuszczonych jonów, które to reagują pomiędzy sobą. W tym samym czasie zostaje naruszona równowaga węglanowo-wapniowa i zaczyna brakować CO2.
Wówczas związki zaczynają szukać punktu, w którym mogą zacząć krystalizować, tzw. jądra krystalizacji. Punkty takie zawsze znajdują się na ścianach rur. Wraz z trwającym odkładaniem się wapna powstaje skorupa nazywana kamieniem.
Składa się on z:
- węglanów wapnia i magnezu (CaCO3, MgCO3)
- siarczanów wapnia i magnezu (CaSO4, MgSO4)
- fosforanów wapnia i magnezu (Ca3(PO4)2, Mg3(PO4)2)
- krzemianów wapnia i magnezu (CaSiO2, MgSiO2)
- wodorotlenku magnezu Mg(OH)2
Osadzanie się kamienia jest niekorzystne, ponieważ stwarza warunki korozyjne, a co za tym idzie wpływa więc na szybsze niszczenie rur i urządzeń. Kamień, osadzając się na rurach, zmniejsza ich przekrój, co jednocześnie powoduje zwiększenie prędkości wody – oba te czynniki wpływają na większe opory przepływu. Większe opory przepływu oznaczają większe spadki ciśnienia. Może się więc okazać, że woda nie dopływa w wystarczającym stopniu do wszystkich odbiorców. Poza tym kamień ma małą przepuszczalność cieplną – osadzając się wewnątrz elementów instalacji grzewczej obniża jej wydajność, ponieważ mniej ciepła może przeniknąć przez pokryte kamieniem ścianki urządzeń. Warstwa kamienia kotłowego o grubości 1 mm powoduje zmniejszenie wydajności o ok. 46%.
Analizując rury użytkowane przez wiele lat, można zauważyć, że kamień zaczyna osadzać się zawsze na kolankach lub rozgałęzieniach i stamtąd rozrasta się w kierunku odcinków prostych. Z chemicznego punktu widzenia, krystalizacja węglanu wapnia przebiega zgodnie z poniższym równaniem:
Ca(HCO3)2 ↔ CaCO3 + H2O + CO2
Powyższa reakcja opisująca tworzenie kamienia może zachodzić także w drugą stronę, tj. kamień może się rozpuszczać. Kierunek, w którym zachodzi reakcja (tworzenia kamienia lub jego rozpuszczanie) zależy od tego w którą stronę zachwiana została równowaga węglanowo-wapniowa: w przypadku nadmiaru CO2, kamień jest rozpuszczany, w przeciwnym wypadku, odkładany. Kierunek zachodzenia tych procesów zależy także od czynników fizycznych: ciśnienia i temperatury.
Powszechnie wiadomo że, prawie wszystkie substancje stałe posiadają strukturę krystaliczną.
Kryształy, ze względu na układ wewnętrzny cząstek w sieci krystalicznej, można podzielić na 7 układów krystalograficznych, w których wyróżnia się 32 klasy krystalograficzne.
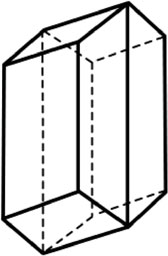
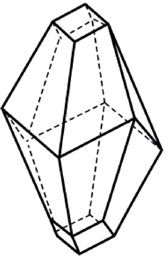
Węglan wapnia CaCO3 występuje w przyrodzie w dwóch postaciach krystalicznych: jako heksagonalny kalcyt i aragonit, który ma budowę rombową. Osad węglanu wapnia wytrącony na gorąco z rozcieńczonych roztworów wykazuje strukturę nietrwałego aragonitu i z biegiem czasu przechodzi w kalcyt. Osad strącony na zimno jest bezpostaciowy i również stopniowo przechodzi w kalcyt. Te struktury krystaliczne są różne, ale powiązane ze sobą. W takim przypadku (tj. gdy struktura chemiczna jest taka sama) o tym jak krystalizuje węglan wapnia decydują warunki termodynamiczne (ciśnienie, temperatura). Jak widać na przedstawionych poniżej rysunkach, w przypadku obu sieci krystalicznych, jedna z osi jest dłuższa niż pozostałe. Oznacza to, że kryształ rośnie w jednym z kierunków szybciej. Szybkość wzrostu jest anizotropiczna, tj. zależna od kierunku.
Oznacza to, że, jeśli kryształy mogą wzrastać w warunkach niezakłóconych, to krystalizują w formy przypominające igły. Jeśli prędkość wzrostu jest taka sama we wszystkich osiach, krystalizują wówczas w formy kuliste. W sieci krystalicznej kalcytu krystalizują także MgCO3 i FeCO3 (stąd ich obecność w kamieniu kotłowym).
Sieć krystaliczna anhydrytu (bezwodny CaSO4) lub gipsu (CaSO4 · 2 H2O) odpowiada sieci krystalicznej kalcytu.
Woda
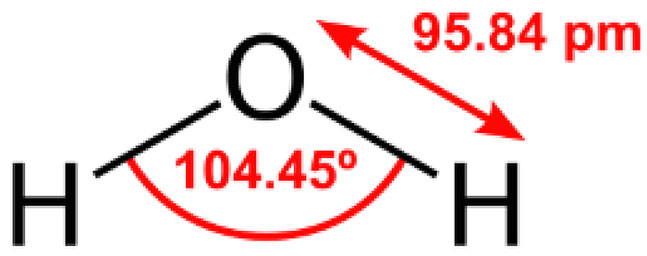
Aby zrozumieć ten proces należy zgłębić kilka informacji o wodzie. W rzucie na płaszczyznęcząsteczka wody ma wygląd trójkąta równoramiennego z atomem tlenu w jednym narożniku trójkąta i atomami wodoru w pozostałych dwóch. Boki tego trójkąta mają długości: 1,013 x 10-10 m (wiązanie H - O) oraz 1,63 x 10-10 m (średnie odległości między atomami wodoru). Kąt między wiązaniami H - O ma wartość 104°27’, co odpowiada 1,82 rad.
W trzech wymiarach cząsteczka wody ma kształt tetraedru z atomem tlenu w środku i atomami wodoru oraz wolnymi parami elektronowymi w wierzchołkach. Cząsteczki wody są nieliniowe, a wiązania H–O są silnie spolaryzowane. Stąd też woda ma trwały moment dipolowy – czyli jest silnie polarna. Na atomie tlenu znajdują się dwie wolne pary elektronowe. Oznacza to, że cząsteczka wody może tworzyć cztery wiązania wodorowe: dwa przez tlen (a konkretnie przez jego wolne pary elektronowe) i dwa przez atomy wodoru mogące oddziaływać z innymi wolnymi parami elektronowymi. Te wiązania wodorowe są odpowiedzialne za łączenie się cząsteczek wody w asocjaty i za powstawanie struktury lodu.
Fizyka i chemia
W wodzie poddanej fizycznemu oczyszczaniu wody zahamowana zostaje krystalizacja węglanów (głównie kalcytu) w wyniku zainicjowania konkurencyjnego procesu, aktywacji koloidalnego roztworu krzemionki, która następnie absorbuje jony wapnia, magnezu i innych metalii wytrąca się jako bezpostaciowy skoagulowany aglomerat (aragonit). Prawdopodobnym mechanizmem aktywacji krzemionki koloidalnej jest deformacja warstwy rozmytej pod wpływem siły Lorentza, co prowadzi do zwiększonego stężenia kationów w warstwie absorpcyjnej ujemnie naładowanej krzemionki.
Istnieje wiele zasad, o które opierają się urządzenia stosowane do fizycznego oczyszczania wody: od magnesów umieszczanych wewnątrz rur po wstrzykiwanie zarodków kryształów do wody, do których przyczepiają się powstające kryształy węglanu wapnia. Zarodek kryształu to próbka monokryształu o określonej orientacji krystalograficznej, wykorzystywana w hodowli monokryształów w celu nadania kryształowi pożądanej orientacji. Użyte w omówionej w tej pracy metodzie, urządzenia zamieniają wodorowęglan wapnia Ca(HCO3)2 w elektrycznie i chemicznie obojętny CaCO3 bezpośrednio w wodzie, a nie na powierzchni rur. Krąży on nadal w wodzie - tyle, że w postaci mulistych osadów, a nie osadza się na ściankach instalacji w postaci kamienia kotłowego. Można to osiągnąć tylko wtedy, jeśli krystalizacja nastąpi zanim woda będzie miała kontakt ze ścianami rur, urządzeniami i zakończeniami sieci. By do tego doprowadzić, muszą być spełnione dwa warunki:
- Jądro krystalizacji musi być obecne w wodzie; jeśli nie jest obecne to należy je wytworzyć,
- Równowaga węglanowo - wapniowa musi zostać naruszona aby z rozpuszczonego wodorowęglanu wytworzył się stały węglan.
Doświadczenia pokazały, że wprowadzenie pola magnetycznego lub elektrycznego do wody pozwala na uzyskanie wymaganych rezultatów, choć z różnym skutkiem. W tej pracy uwaga została skupiona jedynie na wpływie pola elektrycznego.
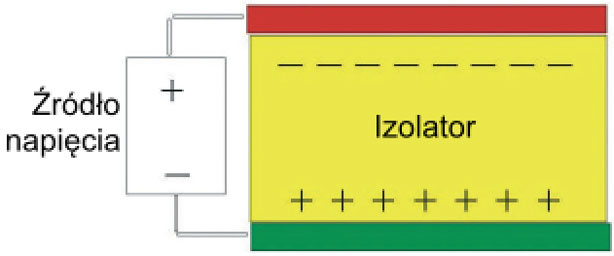
W jaki sposób pole elektryczne może być generowane w rurach z różnych materiałów? Na kolejnym rysunku przedstawiono podstawę procesu elektryzowania dielektryka na przykładzie kondensatora. Jest to element elektryczny (elektroniczny), zbudowany z dwóch przewodników (okładek) rozdzielonych dielektrykiem. Gdy do okładek kondensatora zostanie przyłożone napięcie, w izolatorze (dielektryku) nastąpi rozdzielenie i przyciągnięcie ładunków przeciwnych do przyłożonych do okładek. Innym przykładem elektryzowania ciał przez indukcję jest wprowadzenie dwóch połączonych ze sobą powierzchni przewodnika prostopadle do pola elektrycznego: jedna z powierzchni oddaje wtedy elektrony drugiej. Po rozdzieleniu tych powierzchni jedna z nich jest naładowana dodatnio (niedobór elektronów), a druga ujemnie (nadmiar elektronów).
Na rysunku 6. pokazano jak działa pole elektryczne w rurze metalowej (przewodzącej prąd) i rurze niemetalowej (będącej izolatorem). Efekt końcowy jest taki sam: przy powierzchni rury gromadzą się ładunki przeciwne do polaryzacji zwoju.
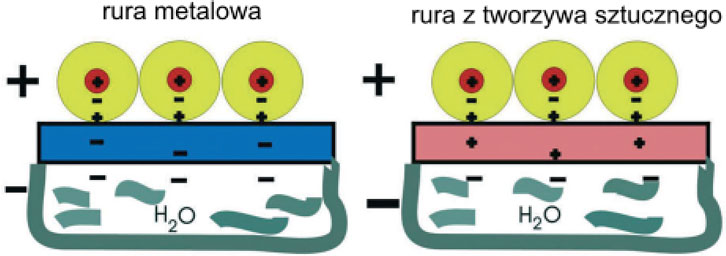
Jeśli cyklicznie będzie dokonywać się zmiany bieguny zwojów (naprzemiennie) lub będzie przykładany biegun i rozładowywane uzwojenie (pulsacyjnie), to wytworzony zostanie tzw. prąd przesunięcia między uzwojeniem a ścianą rury. W ten sposób zostanie wywołany prąd płynący od/z ziemi do ścian rury, gdzie przewodnikiem będzie woda. Takie naprzemienne lub pulsacyjne przykładanie napięcia do uzwojenia wywołuje naprzemienne lub pulsacyjne pole elektryczne wzdłuż rury wraz z wirowym polem magnetycznym centrycznie wokół rury.
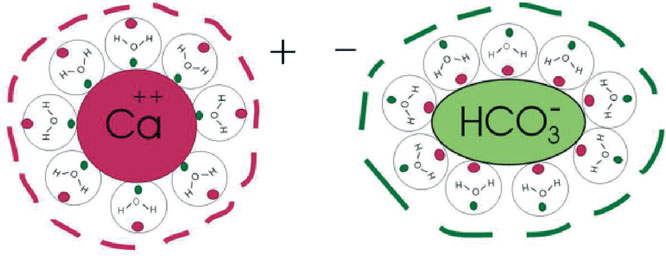
Ważnym aspektem staje się rozpuszczony w wodzie kamień kotłowy (rysunek 6). Rozpuszczony kamień – wodorowęglan wapnia – dysocjuje do jednego, dodatnio naładowanego jonu Ca2+ i dwóch jonów wodorowęglanowych HCO3-. Każdy z jonów otoczony jest „klatką” cząsteczek wody: cząsteczki wody otaczają jon wapniowy w ten sposób, że atomy tlenu są skierowane w stronę jonu wapniowego, natomiast wodoru skierowane są na zewnątrz. Jon wodorowęglanowy jest otoczony cząsteczkami wody w ten sam sposób, z tym, że atomy tlenu są skierowane na zewnątrz. Każda z tych grup utrzymywana jest siłami elektrostatycznymi i charakteryzuje się dodatnim bądź ujemnym ładunkiem elektrycznym co przedstawiono schematycznie na rysunku 8.
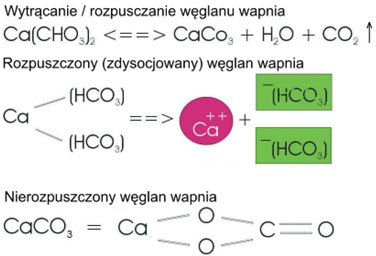
Rysunek 7. Schemat rozpuszczonego w wodzie węglanu wapnia
Te „klatki” wodne powinny być postrzegane jako sfery o średnicy 1-2 nm z ok. 100-200 cząsteczkami wody otaczającymi jon. Masa każdej z grup (zarówno Ca2+ jak i HCO3-) wynosi 30-60 x10-22 g. Jest to bardzo interesujące z punktu widzenia oczyszczania wody.
Wyindukowane zmienne pole elektryczne oddziałuje na jony i na grupy zawarte w wodzie powodując poruszanie się ich w rurze we wszystkich kierunkach. Oscylacje pola elektrycznego powodują oscylacje materii, które rozprzestrzeniają się osiowo (wzdłuż rury). Z fizycznego punktu widzenia jest to podłużna fala mechaniczna. Obszary zwiększonego ciśnienia i ciśnienia ujemnego przeplatają się, co powoduje lokalną adsorpcję CO2. Jeśli częstotliwość oscylacji jest odpowiednia, wtedy „klatki” wodne wokół jonów ulegają rozpadowi co powoduje lokalny spadek stężenia CO2.
Równowaga węglanowo - wapniowa jest miejscami zaburzana. W tym samym czasie poszczególne jony rozpuszczonego węglanu wapnia są uwalniane z „klatek” wodnych. Wówczas mogą się ze sobą połączyć i tworzyć cząsteczki węglanu wapnia, które następnie służą jako jądra krystalizacji. Kolejne cząsteczki są pochłaniane przez takie jądro i rozpoczyna się na nich krystalizacja węglanu wapnia.
Kryształy węglanu wapnia są elektrycznie obojętne i już nie reagują w wodzie. Ponadto, kryształy te nie odkładają się na istniejących złogach na ściankach rur.
Aby opisany powyżej proces mógł zajść, musi być wywołane zmienne pole elektryczne w określonym przedziale częstotliwości, który powoduje drgania rezonansowe „klatek” wodnych. Ponieważ wody wodociągowe spełniające niemieckie wymagania są różne pod względem ilości rozpuszczonych minerałów, pH i przewodności, różne są też warunki powstawania zmiennego pola elektrycznego w rurze. Dodatkowym czynnikiem wpływającym na proces jest zmienna prędkość przepływu wody. Urządzenia pracujące tylko z jedną częstotliwością, oczywiście może przypadkowo zgrać się z częstotliwością rezonansową drgań, ale w większości przypadków będziepracowało nieefektywnie.
Testowane urządzenie Vulcan 5000

Parametry techniczne testowanego urządzenia jak i efekt końcowy procesu są znane, zatem sensownym jest, na podstawie tych informacji określenie teoretycznej i praktycznej efektywności urządzenia.
Stosowane urządzenie wyposażone jest w dwa uzwojenia, które naprzemiennie otrzymują impulsy zmieniane 10 razy na sekundę: 50 ms pulsacji i 50 ms braku pulsacji. Podczas gdy jeden ze zwojów nie ma przyłożonego napięcia, drugi otrzymuje pulsacje o częstotliwości od 3 do 32 kHz.
Urządzenie to jest w stanie oczyszczać 5 m3 wody na godzinę. Oznacza to w przypadku rury ½ cala
szybkość przepływu wody 1,13 cm/ms, natomiast w przypadku rury 1-calowej: 0,28 cm/ms, a w przypadku rury 2-calowej: 0,07 cm/ms. Co zatem z prędkością reakcji? Według Instytutu Maxa - Borna w Berlinie prędkość tworzenia cząstek w wodzie z użyciem matrycy laserowej wynosi od 10-20 x 10-15 s. Czas ten jest niewyobrażalnie mały w stosunku do czasu przebywania cząstek wody w sekcji rury poddawanej działaniu urządzenia.
Warstwy ochronne i inkrustacja
Wiadomo, że płynąca w rurach woda przyspiesza na zakrzywieniach rur. Płynie ona szybciej po zewnętrznej niż po wewnętrznej stronie. Według uproszczonego równania Bernoulli’ego, suma ciśnień statycznego (Pstat) i dynamicznego (Pdyn) jest stała:
Pstat + Pdyn = const
Powyższe równanie to jedno z podstawowych równań hydrodynamiki płynów idealnych, sformułowane przez Daniela Bernoulliego w 1738 roku. Opisuje ono zachowanie gęstości energii całkowitej na linii prądu. Obowiązuje w podstawowej wersji dla stacjonarnego przepływu nieściśliwego płynu idealnego, a w wersji rozszerzonej dla idealnego płynu barotropowego. Wynika ono z zasady zachowania energii i stanowić powinno jej zapis za pomocą parametrów hydrodynamicznych.
W wodzie płynącej ciśnienie dynamiczne wzrasta, a ciśnienie statyczne spada. Oznacza to, że po wewnętrznej stronie rury następuje niedobór CO2 i zostaje naruszona równowaga węglanowo - wapniowa. Węglan wapnia ulega uwolnieniu, znajdując punkty krystalizacji po wewnętrznej stronie rurociągu. W ten sposób warstwa kamienia rośnie odśrodkowo. Razem z węglanem odkładają się również inne minerały. Z powodu zmian ciśnienia, podobna sytuacja występuje na złączeniach/rozgałęzieniach rur. Parująca woda oraz ulatniający się z niej CO2 powoduje też powstawanie kamienia na końcówkach kranów i pryszniców. Na powierzchniach grzewczych usuwany jest CO2 z wody, co powoduje, że stają się one powierzchniami „wybieranymi” jako punkty krystalizacji węglanu wapnia.
Woda wodociągowa, z założenia, jest wodą spełniającą normy wody przeznaczonej do picia. Jest już wodą uzdatnioną. W Polsce najwyższa dopuszczalna twardość ogólna w wodzie do picia wynosi 28°dH (stopni niemieckich). Taka wartość nie jest szkodliwa dla zdrowia, ale oznacza wodę bardzo twardą, która powoduje liczne osady na bateriach, sanitariatach i kamień kotłowy w instalacji. Średnia twardość wody wodociągowej w Polsce wynosi 18°dH, czyli z problemami spowodowanymi twardą wodą spotyka się większość Polaków. Obecność kamienia kotłowego w wodzie do picia jest bardzo ważnym aspektem z dwóch powodów: po pierwsze: woda dostarcza organizmowi ludzkiemu związki wapnia i magnezu, a wiadomo, że do prawidłowego funkcjonowania organizm ludzki potrzebuje nie tylko wody, ale również substancji w niej rozpuszczonych. Po drugie: reszta wodorowęglanowa reaguje z metalem z którego zbudowane są rury tworząc ochronną warstwę metal - wodorowęglan. Zjawisko to jest szczególnie ważne w przypadku zastosowania rur miedzianych. Rysunek 9 a) obrazuje szczegóły warstwy ochronnej. Widać na nich jak grupy kryształów pokrywają powierzchnię rury chroniąc ją przed korozją.

Rysunek 9. Ochronna warstwa rurociągu
Ochronna warstwa rurociągu złożona z:
- węglanu,
- fosforanów oraz
- złogi pyłu węglanowego.
Rysunek 9 b) przedstawia obraz z mikroskopu elektronowego sztucznie powstałej fosforanowej warstwy ochronnej zabezpieczającą przed działaniem zjawiska korozji rur. Fosforany krystalizują w podobne systemy kryształów jak węglany.
Z czasem jednak, pożądana warstwa węglanu wzrasta za bardzo ponieważ stanowi doskonały punkt krystalizacji. Stopniowy wzrost powoduje zatykanie rur, począwszy od zakrętów i rozgałęzień. Jak wspomniano wcześniej, proces odkładania się węglanu rozchodzi się wtedy na proste odcinki rur. Dzieje się tak aż do czasu gdy w wodzie obecny jest węglan wapnia. Większość węglanu transportowana jest przez rury i nie zdąża się osadzić. W 100 m3 wody o twardości 28odH znajduje się około 45 kg węglanu wapnia. Przekształcenie węglanu wapnia w sposób opisany wcześniej spowodowałoby, że zostałby on w formie mikroskopijnych kryształów wymyty z rur, bez możliwości krystalizacji na ich ścianach.
Zastosowanie urządzenia do fizycznego oczyszczania wody pokazało, że kamień nie osadza się nawet na grzałkach w bojlerach/podgrzewaczach wody. Zamiast tego, na dnie zbiornika gromadzi się pył węglanowy (rysunek 9c), natomiast elementy grzejne (grzałki) pozostają czyste. Przykładowe zastosowanie urządzenia pokazało, że w ciągu roku w bojlerze o pojemności 150 litrów zgromadziło się około 2 kg pyłu węglanowego. Natomiast nie zaobserwowano wykształcenia się absolutnie żadnego kamienia na grzałkach. Urządzenie do fizycznego oczyszczania wody zostało także sprawdzone w wymiennikach ciepła w sieciach ciepłowniczych po stronie wtórnej i również się sprawdziło: kamień się nie osadzał (w ciągu 4 lat użytkowania ani razu nie czyszczono ścian rurociągów).
Instalacja urządzenia do fizycznego oczyszczania wody nie sprawia, że węglan wapnia znika, ale czyni go „nieszkodliwym”. Krople wody spadając na powierzchnię, parują, pozostawiając na niej pyłwęglanowy, który może być usunięty przy użyciu wilgotnej szmatki. Jeżeli jednak pył tego typu będzie miał kontakt z powietrzem atmosferycznym i wilgocią dłuższy czas, może pod wpływem CO2 z powietrza ulec rozpuszczeniu w wodzie. W takim przypadku możliwa jest krystalizacja tworząca „zwyczajny” kamień kotłowy.
Usuwanie istniejacego kamienia i ochrona przed korozją
Urządzenia wykorzystywane do fizycznego oczyszczania wody są również zdolne do usuwania istniejącego kamienia oraz zapobiegania powstawaniu rdzy i korozji. Równanie, którym opisano powstawanie kamienia jest reakcją odwracalną.:
Ca(HCO3)2 ↔ CaCO3 + H2O + CO2
Równowaga węglanowo - wapniowa gra tutaj kluczową rolę. Jeśli w roztworze jest nadmiar kwasu węglowego, kamień ulega rozpuszczeniu. Każda krystalizująca cząsteczka węglanu uwalnia do wody jedną cząsteczkę kwasu węglowego. Kwas węglowy stopniowo atakuje i rozpuszcza kamień osadzony na rurach. W zależności od tego w jakim stopniu zakamienione są rury (zależy to od twardości wody i czasu użytkowania rur), proces oczyszczania może trwać od pół roku do roku.
Należy zauważyć, że kamień jest usuwany, a warstwa ochronna rury nie ulega ponownemu rozpuszczeniu. Oczywiście, na ponowne rozpuszczanie narażony jest także węglan wapnia, który skrystalizował bezpośrednio w wodzie na skutek działania urządzenia. Kryształy te są jednak znacznie mniej podatne na to zjawisko, gdyż ich struktura zawiera mniej defektów sieci krystalicznej takich jak: wakanse, atomy międzywęzłowe, podstawienia atomów i cząstek, dyslokacje i defekty warstwowe. Defektem sieci krystalicznej nazywamy niedoskonałości kryształów polegające na punktowym lub warstwowym zerwaniu regularności ich sieci przestrzennej. Defekty występują praktycznie we wszystkich rzeczywistych kryształach. Wynikają one z natury procesu krystalizacji.
Większa ilość defektów sieci krystalicznej w kamieniu zarastającym rury powoduje, iż ma on większą powierzchnię i energię wewnętrzną i dlatego też jest najpierw „atakowany” przez uwolniony CO2. Stopniowe rozpuszczanie kamienia zarastającego rury może czasem powodować odrywanie się widocznych gołym okiem fragmentów kamienia zatrzymujących się następnie na perlatorach.
Omawiane równanie prezentuje stan równowagi, jednak jak wiadomo, w naturze nie istnieje stała równowaga lecz równowaga płynna (co oznacza, że w jednostce czasu tyle samo węglanu wapnia się rozpuszcza co krystalizuje, nawet jeśli nie ma żadnego wpływu czynników zewnętrznych).
Oczywiście proces fizycznego oczyszczania wody nie spowoduje skrystalizowania całości Ca(HCO3)2 w odcinku rury na który ma wpływ, a część rozpuszczonego węglanu przepłynie dalej. Jednakże zaburzenie równowagi węglowodanowo - wapniowej powoduje, iż za miejscem, w którym umieszczono urządzenie do fizycznego oczyszczania wody preferowany jest proces rozpuszczania, zamiast procesu osadzania się węglanu wapnia na ściankach rur, w związku z czym rury za urządzeniem nie zarastają. Dzięki temu, że na ścianach rur nie osadza się kamień kotłowy, możliwe jest, iż warstwa złożona z węglanów metali, chroniąca rury przed korozją, stanie się grubsza.
Doświadczenie pokazuje, że pomimo obecności ochronnej warstwy węglanu metalu występuje zjawisko korozji. Zachodzi ono w przypadku zarówno rur galwanizowanych jak i rur miedzianych.
Zatem jak to się dzieje?
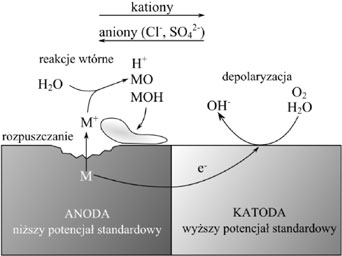
Rysunek 10. Korozja elektrochemiczna żelaza
Na rysunku 10 przedstawiono proces korozji elektrochemicznej żelaza, w przypadku gdy na elemencie żelaznym znajduje się kropla wody i zapewniony jest kontakt z powietrzem. Element żelazny pełni rolę przewodnika elektryczności, zaś kropla wody elektrolitu. Brak kontaktu z tlenem atmosferycznym w punkcie, w którym znajduje się kropla wody i kontakt z nim w miejscu, gdzie kropli nie ma, wytwarza różnicę potencjałów. Brzeg kropli staje się katodą (nadmiar elektronów) natomiast centrum kropli anodą (niedobór elektronów). Na anodzie zachodzi reakcja utleniania metalu: Fe -> Fe2+ + 2e. Zaś na anodzie redukcji: 2 H2O + O2 +2e- -> 2 OH
W przypadku elementów z miedzi mechanizm korozji jest podobny. W przypadku rur, proces korozji przebiega podobnie, z tą różnicą, że zachodzi inny mechanizm kontaktu tlenu z metalem. Schematycznie ten proces przedstawia rysunek 11. W przypadku, gdy woda nie jest poddawana fizycznemu oczyszczaniu, węglan wapnia odkłada się nierównomiernie, według zasad opisanych wcześniej. Między odcinkami o grubej warstwie kamienia a odcinkami bez „miejsc zarośniętych” istnieje różnica w dostępie tlenu rozpuszczonego do powierzchni metalowej. Umożliwia to korozję na tej samej zasadzie jak w przypadku kontaktu z powietrzem atmosferycznym.
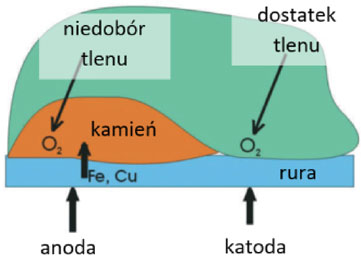
Rysunek 11. Korozja rury metalowej w przypadku kamienia kotłowego o różnej grubośc
Udowodniono, że najczęściej rury korodują w pobliżu kolanek i rozgałęzień, ponieważ w tych miejscach kamień gromadzi się w największej ilości.
Jeśli zostanie usunięty kamień pozostawiając jedynie warstwę ochronną, kontakt z tlenem rozpuszczonym będzie taki sam na całym odcinku rurociągu i nie będzie mogła się wytworzyć różnica potencjału, a tym samym korozja elektrochemiczna nie będzie mogła zajść. Jest to szczególnie istotne w przypadku rur miedzianych, które w przypadku wody bogatej w tlen rozpuszczony i o pH < 6,5 są szczególnie podatne na korozje, zwłaszcza korozję wżerową. Bardzo ważnym aspektem jest równomierna warstwa ochronna w przypadku rur miedzianych, także ze względu na to, że materiał z którego są zbudowane nie jest zazwyczaj zupełnie czysty (zanieczyszczenia metalu ułatwiają korozję). Korozja miedzi ma też bardzo zły wpływ na zdrowie, szczególnie dzieci, gdyż miedź korodująca rury przedostaje się do wody. Nie bez przyczyny miedź nazywana jest „ołowiem XX wieku”.
Podsumowanie
Skuteczność fizycznego oczyszczania wody wynika nie tylko z doświadczeń użytkowników, ale ma również silne podłoże teoretyczne i praktyczne poparte fizyczno-chemicznymi dowodami.
Specyfika pracy omawianego urządzenia wskazuje na to, iż typowe testy laboratoryjne, zwłaszcza te krótkie, często zawodzą lub dostarczają fałszywe rezultaty. Najlepiej byłoby opracować nową procedurę testową, która dostarczyłaby ilościowe dowody przedstawionych w niniejszym opracowaniu teorii.











